Почему химические превращения сопровождаются выделением или поглощением теплоты

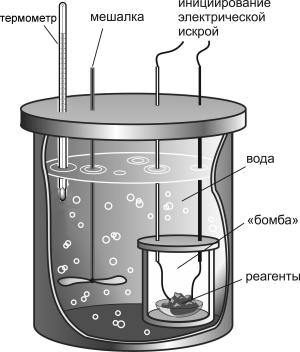
А. Теплота реакции и калориметрия
В отличие от ядерных реакций , при химических реакциях не изменяется общее число ядер атомов и изотопный состав химических элементов. Химические реакции происходят при смешении или физическом контакте реагентов самопроизвольно, при нагревании, участии катализаторов катализ , действии света фотохимические реакции , электрического тока электродные процессы , ионизирующих излучений радиационно-химические реакции , механического воздействия механохимические реакции , в низкотемпературной плазме плазмохимические реакции и т. Взаимодействие молекул между собой происходит по цепному маршруту: ассоциация — электронная изомеризация — диссоциация , в котором активными частицами являются радикалы , ионы , координационно-ненасыщенные соединения. Скорость химической реакции определяется концентрацией активных частиц и разницей между энергиями связи разрываемой и образуемой. Химические процессы, протекающие в веществе, отличаются и от физических процессов, и от ядерных превращений.





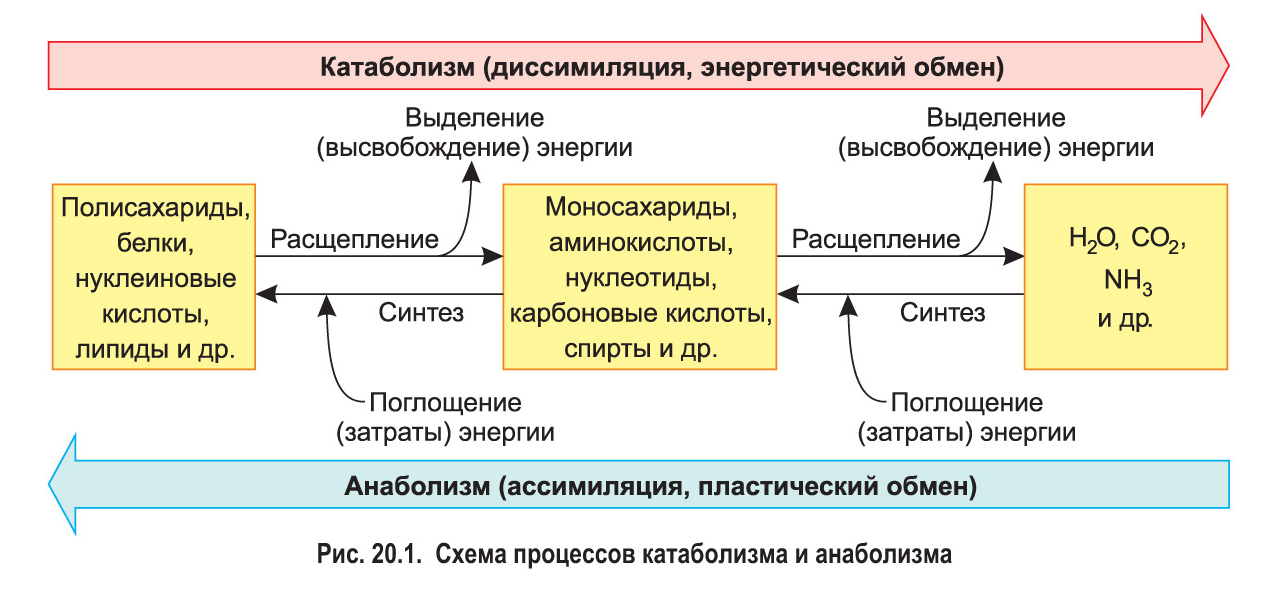
Исходные вещества и продукты реакции обладают разным запасом энергии. Если энергия продуктов меньше энергии исходных веществ, то теплота выделяется в окружающую среду, в противоположном случае теплота поглощается. С выделением теплоты происходят, например, реакции горения. Поглощением теплоты сопровождаются многие реакции разложения, например: разложение карбоната кальция, малахита, воды. Однако реакции разложения дихромата аммония или перманганата калия протекают с выделением теплоты.





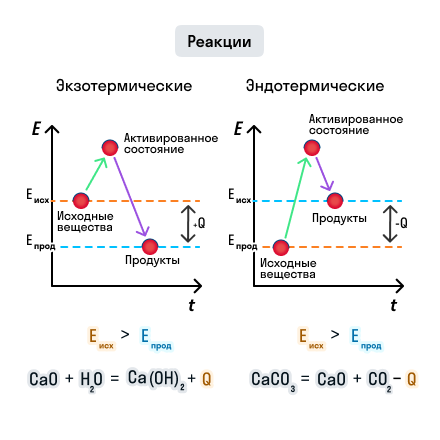
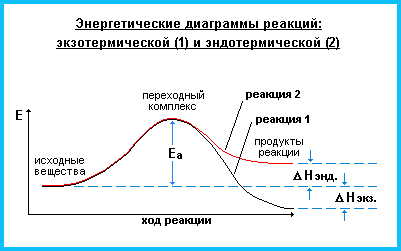



Как известно, большинство химических реакций сопровождаются выделением экзотермические реакции либо поглощением эндотермические реакции теплоты. Первое начало термодинамики дает возможность рассчитать тепловой эффект химической реакции при различных условиях её проведения. Тепловой эффект теплота химической реакции — Q - количество теплоты, выделившейся либо поглотившейся в ходе реакции.